Белки - полимерные молекулы, в которых мономерами служат аминокислоты. В составе белков в организме человека встречают только 20 ?-аминокислот. Одни и те же аминокислоты присутствуют в различных по структуре и функциям белках. Индивидуальность белковых молекул определяется порядком чередования аминокислот в белке. Аминокислоты можно рассматривать как буквы алфавита, при помощи которых, как в слове, записывается информация. Слово несёт информацию, например о предмете или действии, а последовательность аминокислот в белке несёт информацию о построении пространственной структуры и функции данного белка.
Общая структурная особенность аминокислот - наличие амино- и карбоксильной групп, соединённых с одним и тем же?-углеродным атомом. R - радикал аминокислот - в простейшем случае представлен атомом водорода (глицин), но может иметь и более сложное строение.
Все 20 аминокислот в организме человека различаются по строению, размерам и физико-химическим свойствам радикалов, присоединённых к?-углеродному атому.
По химическому строению аминокислоты можно разделить на алифатические, ароматические и гетероциклические (табл. 1-1).

Аминокислоты могут ковалентно связываться друг с другом с помощью пептидных связей. Пептидная связь образуется между а-карбоксильной группой одной аминокислоты и?-аминогруппой другой, т.е. является амидной связью. При этом происходит отщепление молекулы воды.
Пептидные цепи содержат десятки, сотни и тысячи аминокислотных остатков, соединённых прочными пептидными связями. За счёт внутримолекулярных взаимодействий белки образуют определённую гфостранственную структуру, называемую "конформация белков". Линейная последовательность аминокислот в белке содержит информацию о построении трёхмерной пространственной структуры. Различают 4 уровня структурной организации белков, называемых первичной, вторичной, третичной и четвертичной структурами (рис. 1-3). Существуют общие правила, по которым идёт формирование пространственных структур белков.
Аминокислотные остатки в пептидной цепи белков чередуются не случайным образом, а расположены в определённом порядке. Линейную последовательность аминокислотных остатков в полипептидной цепи называют "первичная структура белка". Линейные полипептидные цепи индивидуальных белков за счёт взаимодействия функциональных групп аминокислот приобретают определённую пространственную трёхмерную структуру, называемую"конформация" . Все молекулы индивидуальных белков (т.е. имеющих одинаковую первичную структуру) образуют в растворе одинаковую конформацию. Следовательно, вся информация, необходимая для формирования пространственных структур, находится в первичной структуре белков.
В белках различают 2 основных типа конформации полипептидных цепей: вторичную и третичную структуры.
1. Вторичная структура белков
Вторичная структура белков - пространственная структура, образующаяся в результате взаимодействий между функциональными группами, входящими в состав пептидного остова. При этом пептидные цепи могут приобретать регулярные структуры двух типов: ?-спираль и?-структура.
?-Спираль
В данном типе структуры пептидный остов закручивается в виде спирали за счёт образования водородных связей между атомами кислорода карбонильных групп и атомами азота аминогрупп, входящих в состав пептидных групп через 4 аминокислотных остатка. Водородные связи ориентированы вдоль оси спирали (рис. 1-5). На один виток?-спирали приходится 3,6 аминокислотных остатка.
В образовании водородных связей участвуют практически все атомы кислорода и водорода пептидных групп. В результате?-спираль "стягивается" множеством водородных связей. Несмотря на то, что данные связи относят к разряду слабых, их количество обеспечивает максимально возможную стабильность?-спирали. Так как все гидрофильные группы пептидного остова обычно участвуют в образовании водородных связей, гидрофильность (т.е. способность образовывать водородные связи с водой) ?-спиралей уменьшается, а их гидрофобность увеличивается.
Спиральная структура - наиболее устойчивая конформация пептидного остова, отвечающая минимуму свободной энергии. В результате образования?-спиралей полипептидная цепь укорачивается, но если создать условия для разрыва водородных связей, полипептидная цепь вновь удлинится.
Когда водородные связи образуются между атомами пептидного остова различных полипептидных цепей, их называют межцепочечными связями. Водородные связи, возникающие между линейными участками внутри одной полипептидной цепи, называют внутрицепочечными. В?-структурах водородные связи расположены перпендикулярно полипептидной цепи.
2. Третичная структура белков
Третичная структура белков - трёхмерная пространственная структура, образующаяся за счёт взаимодействий между радикалами аминокислот, которые могут располагаться на значительном расстоянии друг от друга в полипептидной цепи.
Связи, участвующие в формировании третичной структуры белков
Гидрофобные взаимодействия
При укладке полипептидная цепь белка стремится принять энергетически выгодную форму, характеризующуюся минимумом свободной энергии. Поэтому гидрофобные радикалы аминокислот стремятся к объединению внутри глобулярной структуры растворимых в воде белков. Между ними возникают так называемые гидрофобные взаимодействия, а также силы ван дер Ваальса между близко прилегающими друг к другу атомами. В результате внутри белковой глобулы формируетсягидрофобное ядро. Гидрофильные группы пептидного остова при формировании вторичной структуры образуют множество водородных связей, благодаря чему исключается связывание с ними воды и разрушение внутренней, плотной структуры белка.
Ионные и водородные связи
Гидрофильные радикалы аминокислот стремятся образовать водородные связи с водой и поэтому в основном располагаются на поверхности белковой молекулы.
Все гидрофильные группы радикалов аминокислот, оказавшиеся внутри гидрофобного ядра, взаимодействуют друг с другом с помощью ионных и водородных связей (рис. 1-11).
Ионные связи могут возникать между отрицательно заряженными (анионными) карбоксильными группами радикалов аспарагиновой и глутаминовой кислот и положительно заряженными (катионными) группами радикалов лизина, аргинина или гистидина.
Водородные связи возникают между гидрофильными незаряженными группами (такими как -ОН, -CONH 2 , SH-группы) и любыми другими гидрофильными группами. Белки, функционирующие в неполярном (ли-пидном) окружении, например белки мембран, имеют обратное устройство: гидрофильные радикалы аминокислот расположены внутри белка, в то время как гидрофобные аминокислоты локализованы на поверхности молекулы и контактируют с неполярным окружением. В каждом случае радикалы аминокислот занимают наиболее выгодное биоэнергетическое положение.
Ковалентные связи
Третичную структуру некоторых белков стабилизируют дисульфидные связи, образующиеся за счёт взаимодействия SH-групп двух остатков цистеина. Эти два остатка цистеина могут находиться далеко друг от друга в линейной первичной структуре белка, но при формировании третичной структуры они сближаются и образуют прочное ковалентное связывание радикалов.
Четвертичная структура белков
Многие белки содержат в своём составе только одну полипептидную цепь. Такие белки называют мономерами. К мономерным относят и белки, состоящие из нескольких цепей, но соединённых ковалентно, например дисульфидными связями (поэтому инсулин следует рассматривать как мономерный белок).
В то же время существуют белки, состоящие из двух и более полипептидных цепей. После формирования трёхмерной структуры каждой полипептидной цепи они объединяются с помощью тех же слабых взаимодействий, которые участвовали в образовании третичной структуры: гидрофобных, ионных, водородных.
Количество и взаиморасположение полипептидных цепей в пространстве называют "четвертичная структура белков". Отдельные полипептидные цепи в таком белке носят название протомеров, или субъединиц. Белок, содержащий в своём составе несколько протомеров, называют олигомерным.
Все белки с одинаковой первичной структурой, находящиеся в одинаковых условиях, приобретают одинаковую, характерную для данного индивидуального белка конформацию, определяющую его специфическую функцию. Функционально активную конформацию белка называют "нативная структура".
При различных заболеваниях происходит изменение белкового состава тканей. Эти изменения называются протеинопатиями. Различают наследственные и приобретённые протеинопатии. Наследственные протеинопатии развиваются в результате повреждений в генетическом аппарате данного индивидуума. Какой-либо белок не синтезируется вовсе или синтезируется, но его первичная структура изменена. Примеры наследственных протеинопатии - гемоглобинопатии, рассмотренные выше. В зависимости от роли дефектного белка в жизнедеятельности организма, от степени нарушения конформации и функции белков, от гомо- или гетерозиготности индивидуума по этому белку наследственные протеинопатии могут вызывать болезни, протекающие с различной степенью тяжести, вплоть до летального исхода ещё до рождения или в первые месяцы после рождения.
полиморфизм белков - существование разных форм белка, выполняющих одинаковые или очень сходные функции (изобелки). Чаще всего изучают полиморфизм ферментов (т. е. наличие изофер-ментов), поскольку их гораздо легче обнаружить, чем другие белки, по катализируемой ими реакции.
2 .Физико-химические свойства белков
Индивидуальные белки различаются по своим физико-химическим свойствам: форме молекул, молекулярной массе, суммарному заряду
молекулы, соотношению полярных и неполярных групп на поверхности нативной молекулы белка, растворимости белков, а также степени устойчивости к воздействию денатурирующих агентов.
1. Различия белков по форме молекул
Как уже говорилось выше, по форме молекул белки делят на глобулярные и фибриллярные. Глобулярные белки имеют более компактную структуру, их гидрофобные радикалы в большинстве своём спрятаны в гидрофобное ядро, и они значительно лучше растворимы в жидкостях организма, чем фибриллярные белки (исключение составляют мембранные белки).
2. Различия белков по молекулярной массе
Белки - высокомолекулярные соединения, но могут сильно отличаться по молекулярной массе, которая колеблется от 6000 до 1 000 000 Д и выше. Молекулярная масса белка зависит от количества аминокислотных остатков в полипептидной цепи, а для олигомерных белков - и от количества входящих в него протомеров (или субъединиц).
3. Суммарный заряд белков
Белки имеют в своём составе радикалы лизина, аргинина, гистидина, глутаминовой и аспарагиновой кислот, содержащие функциональные группы, способные к ионизации (ионогенные группы). Кроме того, на N- и С-концах полипептидных цепей имеются α-амино- и α-карбоксильная группы, также способные к ионизации. Суммарный заряд белковой молекулы зависит от соотношения ионизированных анионных радикалов Глу и Асп и катионных радикалов Лиз, Apr и Гис.
Степень ионизации функциональных групп этих радикалов зависит от рН среды. При рН раствора около 7 все ионогенные группы белка находятся в ионизированном состоянии. В кислой среде увеличение концентрации протонов (Н+) приводит к подавлению диссоциации карбоксильных групп и уменьшению отрицательного заряда белков: -СОО - + Н + → -СООН. В щелочной среде связывание избытка ОН" с протонами, образующимися при диссоциации NH 3 + с образованием воды, приводит к уменьшению положительного заряда белков:
NH 3 + +ОН - → -NH 2 + H 2 O.
Значение рН, при котором белок приобретает суммарный нулевой заряд, называют "изоэлектрическая точка" и обозначают как pI. В изоэлектрической точке количество положительно и отрицательно заряженных групп белка одинаково, т.е. белок находится в изоэлектрическом состоянии.
Так как большинство белков в клетке имеет в своём составе больше анионогенных групп (-СОО -), то изоэлектрическая точка этих белков лежит в слабокислой среде. Изоэлектрическая точка белков, в составе которых преобладают катионогенные группы, находится в щелочной среде. Наиболее яркий пример таких внутриклеточных белков, содержащих много аргинина и лизина, - гистоны, входящие в состав хроматина.
Белки, имеющие суммарный положительный или отрицательный заряд, лучше растворимы, чем белки, находящиеся в изоэлектрической точке. Суммарный заряд увеличивает количество диполей воды, способных связываться с белковой молекулой, и препятствует контакту одноимённо заряженных молекул, в результате растворимость белков увеличивается. Заряженные белки могут двигаться в электрическом поле: анионные белки, имеющие отрицательный заряд, будут двигаться к положительно заряженному аноду (+), а катионные белки - к отрицательно заряженному катоду (-). Белки, находящиеся в изоэлектрическом состоянии, не перемещаются в электрическом поле.
4. Соотношение полярных и неполярных групп на поверхности нативных молекул белков
На поверхности большинства внутриклеточных белков преобладают полярные радикалы, однако соотношение полярных и неполярных групп отлично для разных индивидуальных белков. Так, протомеры олигомерных белков в области контактов друг с другом часто содержат гидрофобные радикалы. Поверхности белков, функционирующих в составе мембран или прикрепляющиеся к ним в процессе функционирования, также обогащены гидрофобными радикалами. Такие белки лучше растворимы в липидах, чем в воде.
О том, что такое белки, сейчас знает практически каждый из школьных уроков биологии. Они выполняют множество функций в клетке живого существа.
Что такое белки?
Это сложные органические соединения. Они состоят из аминокислот, которых всего существует 20, однако, соединив их в разной последовательности, можно получить миллионы разнообразных химических веществ.
Структура белков
Когда мы уже знаем, что такое белки, можно подробнее рассмотреть их строение. Существует первичная, вторичная, третичная и четвертичная структура такого рода веществ.
Первичная структура
Это цепь, в которой аминокислоты соединены в нужном порядке. Это чередование и определяет вид белка. Для каждого вещества данного класса оно индивидуально. От первичной структуры во многом зависят также физические и химические свойства того или иного белка.
Вторичная структура
Это пространственная форма, которую принимает полипептидная цепь за счет образования водородных связей между карбоксильными группами и имино-группами. Существует два наиболее распространенных ее типа: альфа-спираль и бета-структура, имеющая лентообразный вид. Первая формируется вследствие возникновения связей между молекулами одной и той же полипептидной цепи, вторая — между двумя или более расположенными параллельно цепями. Однако также возможно возникновение бета-структуры и в пределах одного полимера — в том случае, когда определенные его фрагменты повернуты на 180 градусов.

Третичная структура
Это чередование и расположение относительно друг друга в пространстве участков альфа-спирали, простых полипептидных цепей и бета-структур.
Четвертичная структура
Ее также существует два вида: глобулярная и фибриллярная. Такая структура формируется за счет электростатических взаимодействий и водородных связей. Глобулярная имеет форму небольшого клубка, а фибриллярная — нити. Примерами белков с четвертичной структурой первого типа могут служить альбумин, инсулин, иммуноглобулин и т. д.; фибриллярных — фиброин, кератин, коллаген и другие. Есть и еще более сложные по строению белки, к примеру, миозин, содержащийся в мышечных тканях, он имеет стержень фибриллярной формы, на котором расположены две глобулярные головки.
Химический состав белков

Аминокислотный состав белков может быть представлен двадцатью аминокислотами, которые комбинируются в различном порядке и количестве.
Это глицин, аланин, валин, лейцин, изолейцин, серин, треонин, цистеин, метионин, лизин, аргинин, аспарагиновая кислота, аспарагин, глутаминовая кислота, глутамин, фенилаланин, тирозин, триптофан, гистидин и пролин. Среди них есть незаменимые, то есть те, которые организм человека не в состоянии вырабатывать самостоятельно. Таких аминокислот насчитывается 8 для взрослых и еще 2 для детей: лейцин, изолейцин, валин, метионин, лизин, триптофан, фенилаланин, треонин, а также гистидин и аргинин.
Примеры белков с разной структурой
Ярким представителем глобулярных белков является альбумин. Его третичная структура состоит из альфа-спиралей, которые соединяются одиночными полипептидными цепочками.

Первичная же образуется такими аминокислотами, как аспаргиновая кислота, аланин, цистеин и глицин. Данный белок находится в плазме крови и выполняет функцию транспорта определенных веществ. Из фибриллярных можно выделить фиброин и коллаген. Третичная структура первого представляет собой вещество из бета-структур, которые соединены одиночными полипептидными цепочками. Сама цепь представляет собой чередование аланина, глицина, цистеина и серина. Данное химическое соединение является основным компонентом паутины и шелка, а также перьев птиц.
Что такое денатурация?
Это процесс разрушения сперва четвертичной, затем третичной и вторичной структур белка. Белок, с которым это случилось, уже не может выполнять свои функции и теряет основные физические и химические свойства. Такой процесс происходит в основном из-за воздействия высоких температур или агрессивных химических веществ. К примеру, при температуре выше сорока градусов Цельсия начинает денатурировать гемоглобин, переносящий кислород по крови организмов. Вот почему для человека опасно столь сильное повышение температуры.

Функции белков
Узнав о том, что такое белки, можно обратить внимание на роль этих веществ в жизни клетки и всего организма в целом. Они выполняют девять основных функций. Первая — пластическая. Они являются компонентами многих структур живого организма и служат в качестве строительного материала для клетки. Вторая — транспортная. Белки способны переносить вещества, примером веществ данного назначения являются альбумин, гемоглобин, а также разнообразные белки-транспортеры, находящиеся на плазматической мембране клетки, каждый из которых пропускает только определенное вещество в цитоплазму из окружающей среды. Третья функция — защитная. Ее выполняют иммуноглобулины, которые являются частью иммунной системы, и коллаген, являющийся основным компонентом кожного покрова. Также белки в организме человека и других организмов выполняют регуляторную функцию, так как существует некоторое количество гормонов, представленных такого рода веществами, к примеру, как инсулин. Еще одна роль, выполняемая этими химическими соединениями, — сигнальная. Данные вещества передают электрические импульсы из клетки в клетку. Шестая функция — двигательная. Яркими представителями белков, выполняющих ее, являются актин и миозин, которые способны сокращаться (они находятся в мышцах). Такие вещества могут также служить запасными, однако в таких целях они используются довольно редко, в основном это белки, которые есть в молоке. Они выполняют еще и каталитическую функцию — в природе есть ферменты белковой природы. И последняя функция— рецепторная. Существует группа белков, которые частично денатурируют под воздействием того или иного фактора, давая таким образом сигнал всей клетке, которая передает его дальше.
Л инейные полипептидные цепи индивидуальных белков за счёт взаимодействия функциональных групп аминокислот приобретают определённую пространственную трёхмерную структуру, называемую "конформация". Все молекулы индивидуальных белков (т.е. имеющих одинаковую первичную структуру) образуют в растворе одинаковую конформацию. Следовательно, вся информация, необходимая для формирования пространственных структур, находится в первичной структуре белков.
В белках различают 2 основных типа конформации полипептидных цепей: вторичную и третичную структуры.
2. Вторичная структура белков - пространственная структура, образующаяся в результате взаимодействия между функциональными группами пептидного остова.
При этом пептидные цепи могут приобретать регулярные структуры двух типов: α-спирали
β-структрура Под β-структурой понимают фигуру, подобную листу, сложенному «гармошкой». Фигура формируется за счет образования множества водородных связей между атомами пептидных групп линейных областей одной полипептидной цепи, делающей изгибы, или между разными полипептидными группами.
Связи - водородные, они стабилизируют отдельные фрагменты макромолекул.
3. Третичная структура белков - трёхмерная пространственная структура, образующаяся за счёт взаимодействий между радикалами аминокислот, которые могут располагаться на значительном расстоянии друг от друга в полипептидной цепи.
Структурно состоит из элементов вторичной структуры, стабилизированных различными типами взаимодействий, в которых гидрофобные взаимодействия играют важнейшую роль
стабилизации третичной структуры белка принимают участие:
· ковалентные связи (между двумя остатками цистеина - дисульфидные мостики);
· ионные связи между противоположно заряженными боковыми группами аминокислотных остатков;
· водородные связи;
· гидрофильно-гидрофобные взаимодействия. При взаимодействии с окружающими молекулами воды белковая молекула «стремится» свернуться так, чтобы неполярные боковые группы аминокислот оказались изолированы от водного раствора; на поверхности молекулы оказываются полярные гидрофильные боковые группы.
4. Четвертичной структурой называют взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса. Белковые молекулы, входящие в состав белка с четвертичной структурой, образуются на рибосомах по отдельности и лишь после окончания синтеза образуют общую надмолекулярную структуру. В состав белка с четвертичной структурой могут входить как идентичные, так и различающиеся полипептидные цепочки. В стабилизации четвертичной структуры принимают участие те же типы взаимодействий, что и в стабилизации третичной . Надмолекулярные белковые комплексы могут состоять из десятков молекул.
Роль.
Образование пептидов в организме происходит в течение нескольких минут, химический же синтез в условиях лаборатории - достаточно длительный процесс, который может занимать несколько дней, а разработка технологии синтеза – несколько лет. Однако, несмотря на это, существуют довольно весомые аргументы в пользу проведения работ по синтезу аналогов природных пептидов. Во-первых, путём химической модификации пептидов возможно подтвердить гипотезу первичной структуры. Аминокислотные последовательности некоторых гормонов стали известны именно благодаря синтезу их аналогов в лаборатории.
Во-вторых, синтетические пептиды позволяют подробнее изучить связь между структурой аминокислотной последовательности и её активностью. Для выяснения связи между конкретной структурой пептида и его биологической активностью была проведена огромная работа по синтезу не одной тысячи аналогов. В результате удалось выяснить, что замена лишь одной аминокислоты в структуре пептида способна в несколько раз увеличить его биологическую активность или изменить её направленность. А изменение длины аминокислотной последовательности помогает определить расположение активных центров пептида и участка рецепторного взаимодействия.
В-третьих, благодаря модификации исходной аминокислотной последовательности, появилась возможность получать фармакологические препараты. Создание аналогов природных пептидов позволяет выявить более «эффективные» конфигурации молекул, которые усиливают биологическое действие или делают его более продолжительным.
В-четвёртых, химический синтез пептидов экономически выгоден. Большинство терапевтических препаратов стоили бы в десятки раз больше, если бы были сделаны на основе природного продукта.
Зачастую активные пептиды в природе обнаруживаются лишь в нанограммовых количествах. Плюс к этому, методы очистки и выделения пептидов из природных источников не могут полностью разделить искомую аминокислотную последовательность с пептидами противоположного или же иного действия. А в случае специфических пептидов, синтезируемых организмом человека, получить их возможно лишь путём синтеза в лабораторных условиях.
57. Классификация белков: простые и сложные, глобулярные и фибриллярные, мономерные и олигомерные. Функции белков в организме .
Классификация по типу строения
По общему типу строения белки можно разбить на три группы:
1. Фибриллярные белки - образуют полимеры, их структура обычно высокорегулярна и поддерживается, в основном, взаимодействиями между разными цепями. Они образуют микрофиламенты, микротрубочки, фибриллы, поддерживают структуру клеток и тканей. К фибриллярным белкам относятся кератин и коллаген.
2. Глобулярные белки - водорастворимы, общая форма молекулы более или менее сферическая.
3. Мембранные белки - имеют пересекающие клеточную мембрану домены, но части их выступают из мембраны в межклеточное окружение и цитоплазму клетки. Мембранные белки выполняют функцию рецепторов, то есть осуществляют передачу сигналов, а также обеспечивают трансмембранный транспорт различных веществ. Белки-транспортёры специфичны, каждый из них пропускает через мембрану только определённые молекулы или определённый тип сигнала.
Простые белки , Сложные белки
Помимо пептидных цепей, в состав многих белков входят и неаминокислотные группы, и по этому критерию белки делят на две большие группы - простые и сложные белки (протеиды). Простые белки состоят только из полипептидных цепей, сложные белки содержат также неаминокислотные, или простетические, группы.
Простые.
Среди глобулярных белков можно выделить:
1. альбумины - растворимы в воде в широком интервале рН (от 4 до 8,5), осаждаются 70-100%-ным раствором сульфата аммония;
2. полифункциональные глобулины с большей молекулярной массой, труднее растворимы в воде, растворимы в солевых растворах, часто содержат углеводную часть;
3. гистоны - низкомолекулярные белки с высоким содержанием в молекуле остатков аргинина и лизина, что обусловливает их основные свойства;
4. протамины отличаются еще более высоким содержанием аргинина (до 85 %), как и гистоны, образуют устойчивые ассоциаты с нуклеиновыми кислотами, выступают как регуляторные и репрессорные белки - составная часть нуклеопротеинов;
5. проламины характеризуются высоким содержанием глутаминовой кислоты (30-45 %) и пролина (до 15 %), нерастворимы в воде, растворяются в 50-90 % этаноле;
6. глутелины содержат около 45 % глутаминовой кислоты, как и проламины, чаще содержатся в белках злаков.
Фибриллярные белки характеризуются волокнистой структурой, практически нерастворимы в воде и солевых растворах. Полипептидные цепи в молекулах расположены параллельно одна другой. Участвуют в образовании структурных элементов соединительной ткани (коллагены, кератины, эластины).
Сло́жные белки́
(протеиды , холопротеины ) - двухкомпонентные белки, в которых помимо пептидных цепей (простого белка) содержится компонент неаминокислотной природы - простетическая группа. При гидролизе сложных белков, кроме аминокислот, освобождается небелковая часть или продукты её распада.
В качестве простетической группы могут выступать различные органические (липиды, углеводы) и неорганические (металлы) вещества.
В зависимости от химической природы простетических групп среди сложных белков выделяют следующие классы :
· Гликопротеиды, содержащие в качестве простетической группы ковалентно связанные углеводные остатки и их подкласс - протеогликаны, с мукополисахаридными простетическими группами. В образовании связи с углеводными остатками обычно участвуют гидроксильные группы серина или треонина. Большая часть внеклеточных белков, в частности, иммуноглобулины - гликопротеиды. В протеогликанах углеводная часть составляет ~95 %, они являются основным компонентом межклеточного матрикса.
· Липопротеиды, содержащие в качестве простетической части нековалентно связанные липиды. Липопротеиды, образованные белками-аполипопротеинами связывающимися с ними липидами и выполняют функцию транспорта липидов.
· Металлопротеиды, содержащие негемовые координационно связанные ионы металлов. Среди металлопротеидов есть белки, выполняющие депонирующие и транспортные функции (например, железосодержащие ферритин и трансферрин) и ферменты (например, цинксодержащая карбоангидраза и различные супероксиддисмутазы, содержащие в качестве активных центров ионы меди, марганца, железа и других металлов)
· Нуклеопротеиды, содержащие нековалентно связанные ДНК или РНК, в частности, хроматин, из которого состоят хромосомы, является нуклеопротеидом .
· Фосфопротеиды, содержащие в качестве простетической группы ковалентно связанные остатки фосфорной кислоты. В образовании сложноэфирной связи с фосфатом участвуют гидроксильные группы серина или треонина, фосфопротеинами являются, в частности, казеин молока :
· Хромопротеиды - собирательное название сложных белков с окрашенными простетическими группами различной химической природы. К ним относится множество белков с металлсодержащейпорфириновой простетической группой, выполняющие разнообразные функции - гемопротеины (белки, содержащие в качестве простетической группы гем - гемоглобин, цитохромы и др.), хлорофиллы;флавопротеиды с флавиновой группой, и др.
1. Структурная функция
2. Защитная функция
3. Регуляторная функция
4. Сигнальная функция
5. Транспортная функция
6. Запасная (резервная) функция
7. Рецепторная функция
8. Моторная (двигательная) функция
Белки — высокомолекулярные органические соединения, состоящие из остатков α-аминокислот.
В состав белков входят углерод, водород, азот, кислород, сера. Часть белков образует комплексы с другими молекулами, содержащими фосфор, железо, цинк и медь.
Белки обладают большой молекулярной массой: яичный альбумин — 36 000, гемоглобин — 152 000, миозин — 500 000. Для сравнения: молекулярная масса спирта — 46, уксусной кислоты — 60, бензола — 78.
Аминокислотный состав белков
Белки — непериодические полимеры, мономерами которых являются α-аминокислоты . Обычно в качестве мономеров белков называют 20 видов α-аминокислот, хотя в клетках и тканях их обнаружено свыше 170.
В зависимости от того, могут ли аминокислоты синтезироваться в организме человека и других животных, различают: заменимые аминокислоты — могут синтезироваться; незаменимые аминокислоты — не могут синтезироваться. Незаменимые аминокислоты должны поступать в организм вместе с пищей. Растения синтезируют все виды аминокислот.
В зависимости от аминокислотного состава, белки бывают: полноценными — содержат весь набор аминокислот; неполноценными — какие-то аминокислоты в их составе отсутствуют. Если белки состоят только из аминокислот, их называют простыми . Если белки содержат помимо аминокислот еще и неаминокислотный компонент (простетическую группу), их называют сложными . Простетическая группа может быть представлена металлами (металлопротеины), углеводами (гликопротеины), липидами (липопротеины), нуклеиновыми кислотами (нуклеопротеины).
Все аминокислоты содержат : 1) карбоксильную группу (-СООН), 2) аминогруппу (-NH 2), 3) радикал или R-группу (остальная часть молекулы). Строение радикала у разных видов аминокислот — различное. В зависимости от количества аминогрупп и карбоксильных групп, входящих в состав аминокислот, различают: нейтральные аминокислоты , имеющие одну карбоксильную группу и одну аминогруппу; основные аминокислоты , имеющие более одной аминогруппы; кислые аминокислоты , имеющие более одной карбоксильной группы.
Аминокислоты являются амфотерными соединениями , так как в растворе они могут выступать как в роли кислот, так и оснований. В водных растворах аминокислоты существуют в разных ионных формах.
Пептидная связь
Пептиды — органические вещества, состоящие из остатков аминокислот, соединенных пептидной связью.
Образование пептидов происходит в результате реакции конденсации аминокислот. При взаимодействии аминогруппы одной аминокислоты с карбоксильной группой другой между ними возникает ковалентная азот-углеродная связь, которую и называют пептидной . В зависимости от количества аминокислотных остатков, входящих в состав пептида, различают дипептиды, трипептиды, тетрапептиды и т.д. Образование пептидной связи может повторяться многократно. Это приводит к образованию полипептидов . На одном конце пептида находится свободная аминогруппа (его называют N-концом), а на другом — свободная карбоксильная группа (его называют С-концом).

Пространственная организация белковых молекул
Выполнение белками определенных специфических функций зависит от пространственной конфигурации их молекул, кроме того, клетке энергетически невыгодно держать белки в развернутой форме, в виде цепочки, поэтому полипептидные цепи подвергаются укладке, приобретая определенную трехмерную структуру, или конформацию. Выделяют 4 уровня пространственной организации белков .
Первичная структура белка — последовательность расположения аминокислотных остатков в полипептидной цепи, составляющей молекулу белка. Связь между аминокислотами — пептидная.

Если молекула белка состоит всего из 10 аминокислотных остатков, то число теоретически возможных вариантов белковых молекул, отличающихся порядком чередования аминокислот, — 10 20 . Имея 20 аминокислот, можно составить из них еще большее количество разнообразных комбинаций. В организме человека обнаружено порядка десяти тысяч различных белков, которые отличаются как друг от друга, так и от белков других организмов.
Именно первичная структура белковой молекулы определяет свойства молекул белка и ее пространственную конфигурацию. Замена всего лишь одной аминокислоты на другую в полипептидной цепочке приводит к изменению свойств и функций белка. Например, замена в β-субъединице гемоглобина шестой глутаминовой аминокислоты на валин приводит к тому, что молекула гемоглобина в целом не может выполнять свою основную функцию — транспорт кислорода; в таких случаях у человека развивается заболевание — серповидноклеточная анемия.
Вторичная структура — упорядоченное свертывание полипептидной цепи в спираль (имеет вид растянутой пружины). Витки спирали укрепляются водородными связями, возникающими между карбоксильными группами и аминогруппами. Практически все СО- и NН-группы принимают участие в образовании водородных связей. Они слабее пептидных, но, повторяясь многократно, придают данной конфигурации устойчивость и жесткость. На уровне вторичной структуры существуют белки: фиброин (шелк, паутина), кератин (волосы, ногти), коллаген (сухожилия).



Третичная структура — укладка полипептидных цепей в глобулы, возникающая в результате возникновения химических связей (водородных, ионных, дисульфидных) и установления гидрофобных взаимодействий между радикалами аминокислотных остатков. Основную роль в образовании третичной структуры играют гидрофильно-гидрофобные взаимодействия. В водных растворах гидрофобные радикалы стремятся спрятаться от воды, группируясь внутри глобулы, в то время как гидрофильные радикалы в результате гидратации (взаимодействия с диполями воды) стремятся оказаться на поверхности молекулы. У некоторых белков третичная структура стабилизируется дисульфидными ковалентными связями, возникающими между атомами серы двух остатков цистеина. На уровне третичной структуры существуют ферменты, антитела, некоторые гормоны.

Четвертичная структура характерна для сложных белков, молекулы которых образованы двумя и более глобулами. Субъединицы удерживаются в молекуле благодаря ионным, гидрофобным и электростатическим взаимодействиям. Иногда при образовании четвертичной структуры между субъединицами возникают дисульфидные связи. Наиболее изученным белком, имеющим четвертичную структуру, является гемоглобин . Он образован двумя α-субъединицами (141 аминокислотный остаток) и двумя β-субъединицами (146 аминокислотных остатков). С каждой субъединицей связана молекула гема, содержащая железо.
Если по каким-либо причинам пространственная конформация белков отклоняется от нормальной, белок не может выполнять свои функции. Например, причиной «коровьего бешенства» (губкообразной энцефалопатии) является аномальная конформация прионов — поверхностных белков нервных клеток.
Свойства белков
Аминокислотный состав, структура белковой молекулы определяют его свойства . Белки сочетают в себе основные и кислотные свойства, определяемые радикалами аминокислот: чем больше кислых аминокислот в белке, тем ярче выражены его кислотные свойства. Способность отдавать и присоединять Н + определяют буферные свойства белков ; один из самых мощных буферов — гемоглобин в эритроцитах, поддерживающий рН крови на постоянном уровне. Есть белки растворимые (фибриноген), есть нерастворимые, выполняющие механические функции (фиброин, кератин, коллаген). Есть белки активные в химическом отношении (ферменты), есть химически неактивные, устойчивые к воздействию различных условий внешней среды и крайне неустойчивые.
Внешние факторы (нагревание, ультрафиолетовое излучение, тяжелые металлы и их соли, изменения рН, радиация, обезвоживание)
могут вызывать нарушение структурной организации молекулы белка. Процесс утраты трехмерной конформации, присущей данной молекуле белка, называют денатурацией . Причиной денатурации является разрыв связей, стабилизирующих определенную структуру белка. Первоначально рвутся наиболее слабые связи, а при ужесточении условий и более сильные. Поэтому сначала утрачивается четвертичная, затем третичная и вторичная структуры. Изменение пространственной конфигурации приводит к изменению свойств белка и, как следствие, делает невозможным выполнение белком свойственных ему биологических функций. Если денатурация не сопровождается разрушением первичной структуры, то она может быть обратимой , в этом случае происходит самовосстановление свойственной белку конформации. Такой денатурации подвергаются, например, рецепторные белки мембраны. Процесс восстановления структуры белка после денатурации называется ренатурацией . Если восстановление пространственной конфигурации белка невозможно, то денатурация называется необратимой .
Функции белков
| Функция | Примеры и пояснения |
|---|---|
| Строительная | Белки участвуют в образовании клеточных и внеклеточных структур: входят в состав клеточных мембран (липопротеины, гликопротеины), волос (кератин), сухожилий (коллаген) и т.д. |
| Транспортная | Белок крови гемоглобин присоединяет кислород и транспортирует его от легких ко всем тканям и органам, а от них в легкие переносит углекислый газ; в состав клеточных мембран входят особые белки, которые обеспечивают активный и строго избирательный перенос некоторых веществ и ионов из клетки во внешнюю среду и обратно. |
| Регуляторная | Гормоны белковой природы принимают участие в регуляции процессов обмена веществ. Например, гормон инсулин регулирует уровень глюкозы в крови, способствует синтезу гликогена, увеличивает образование жиров из углеводов. |
| Защитная | В ответ на проникновение в организм чужеродных белков или микроорганизмов (антигенов) образуются особые белки — антитела, способные связывать и обезвреживать их. Фибрин, образующийся из фибриногена, способствует остановке кровотечений. |
| Двигательная | Сократительные белки актин и миозин обеспечивают сокращение мышц у многоклеточных животных. |
| Сигнальная | В поверхностную мембрану клетки встроены молекулы белков, способных изменять свою третичную структуру в ответ на действие факторов внешней среды, таким образом осуществляя прием сигналов из внешней среды и передачу команд в клетку. |
| Запасающая | В организме животных белки, как правило, не запасаются, исключение: альбумин яиц, казеин молока. Но благодаря белкам в организме могут откладываться про запас некоторые вещества, например, при распаде гемоглобина железо не выводится из организма, а сохраняется, образуя комплекс с белком ферритином. |
| Энергетическая | При распаде 1 г белка до конечных продуктов выделяется 17,6 кДж. Сначала белки распадаются до аминокислот, а затем до конечных продуктов — воды, углекислого газа и аммиака. Однако в качестве источника энергии белки используются только тогда, когда другие источники (углеводы и жиры) израсходованы. |
| Каталитическая | Одна из важнейших функций белков. Обеспечивается белками — ферментами, которые ускоряют биохимические реакции, происходящие в клетках. Например, рибулезобифосфаткарбоксилаза катализирует фиксацию СО 2 при фотосинтезе. |
Ферменты
Ферменты , или энзимы , — особый класс белков, являющихся биологическими катализаторами. Благодаря ферментам биохимические реакции протекают с огромной скоростью. Скорость ферментативных реакций в десятки тысяч раз (а иногда и в миллионы) выше скорости реакций, идущих с участием неорганических катализаторов. Вещество, на которое оказывает свое действие фермент, называют субстратом .
Ферменты — глобулярные белки, по особенностям строения ферменты можно разделить на две группы: простые и сложные. Простые ферменты являются простыми белками, т.е. состоят только из аминокислот. Сложные ферменты являются сложными белками, т.е. в их состав помимо белковой части входит группа небелковой природы — кофактор . У некоторых ферментов в качестве кофакторов выступают витамины. В молекуле фермента выделяют особую часть, называемую активным центром. Активный центр — небольшой участок фермента (от трех до двенадцати аминокислотных остатков), где и происходит связывание субстрата или субстратов с образованием фермент-субстратного комплекса. По завершении реакции фермент-субстратный комплекс распадается на фермент и продукт (продукты) реакции. Некоторые ферменты имеют (кроме активного) аллостерические центры — участки, к которым присоединяются регуляторы скорости работы фермента (аллостерические ферменты ).

Для реакций ферментативного катализа характерны: 1) высокая эффективность, 2) строгая избирательность и направленность действия, 3) субстратная специфичность, 4) тонкая и точная регуляция. Субстратную и реакционную специфичность реакций ферментативного катализа объясняют гипотезы Э. Фишера (1890 г.) и Д. Кошланда (1959 г.).
Э. Фишер (гипотеза «ключ-замок») предположил, что пространственные конфигурации активного центра фермента и субстрата должны точно соответствовать друг другу. Субстрат сравнивается с «ключом», фермент — с «замком».
Д. Кошланд (гипотеза «рука-перчатка») предположил, что пространственное соответствие структуры субстрата и активного центра фермента создается лишь в момент их взаимодействия друг с другом. Эту гипотезу еще называют гипотезой индуцированного соответствия .
Скорость ферментативных реакций зависит от: 1) температуры, 2) концентрации фермента, 3) концентрации субстрата, 4) рН. Следует подчеркнуть, что поскольку ферменты являются белками, то их активность наиболее высока при физиологически нормальных условиях.
Большинство ферментов может работать только при температуре от 0 до 40 °С. В этих пределах скорость реакции повышается примерно в 2 раза при повышении температуры на каждые 10 °С. При температуре выше 40 °С белок подвергается денатурации и активность фермента падает. При температуре, близкой к точке замерзания, ферменты инактивируются.
При увеличении количества субстрата скорость ферментативной реакции растет до тех пор, пока количество молекул субстрата не станет равным количеству молекул фермента. При дальнейшем увеличении количества субстрата скорость увеличиваться не будет, так как происходит насыщение активных центров фермента. Увеличение концентрации фермента приводит к усилению каталитической активности, так как в единицу времени преобразованиям подвергается большее количество молекул субстрата.

Для каждого фермента существует оптимальное значение рН, при котором он проявляет максимальную активность (пепсин — 2,0, амилаза слюны — 6,8, липаза поджелудочной железы — 9,0). При более высоких или низких значениях рН активность фермента снижается. При резких сдвигах рН фермент денатурирует.
Скорость работы аллостерических ферментов регулируется веществами, присоединяющимися к аллостерическим центрам. Если эти вещества ускоряют реакцию, они называются активаторами , если тормозят — ингибиторами .
Классификация ферментов
По типу катализируемых химических превращений ферменты разделены на 6 классов:
- оксиредуктазы (перенос атомов водорода, кислорода или электронов от одного вещества к другому — дегидрогеназа),
- трансферазы (перенос метильной, ацильной, фосфатной или аминогруппы от одного вещества к другому — трансаминаза),
- гидролазы (реакции гидролиза, при которых из субстрата образуются два продукта — амилаза, липаза),
- лиазы (негидролитическое присоединение к субстрату или отщепление от него группы атомов, при этом могут разрываться связи С-С, С-N, С-О, С-S — декарбоксилаза),
- изомеразы (внутримолекулярная перестройка — изомераза),
- лигазы (соединение двух молекул в результате образования связей С-С, С-N, С-О, С-S — синтетаза).
Классы в свою очередь подразделены на подклассы и подподклассы. В действующей международной классификации каждый фермент имеет определенный шифр, состоящий из четырех чисел, разделенных точками. Первое число — класс, второе — подкласс, третье — подподкласс, четвертое — порядковый номер фермента в данном подподклассе, например, шифр аргиназы — 3.5.3.1.
Перейти к лекции №2 «Строение и функции углеводов и липидов»
Перейти к лекции №4 «Строение и функции нуклеиновых кислот АТФ»
Белки представляют собой органические высокомолекулярные соединения. Эти вещества также называют протеинами, полипептидами. Далее рассмотрим, каковы структура и функции белков.
Общие сведения
Химическая структура белков представлена альфа-аминокислотами, соединенными в цепочку посредством пептидной связи. В живых организмах состав определяет генетический код. В процессе синтеза в большинстве случаев применяется 20 аминокислот стандартного типа. Множеством их комбинаций формируются белковые молекулы с самыми разнообразными свойствами. Аминокислотные остатки часто подвергаются посттрансляционным модификациям. Они могут возникнуть и до того, как белок станет выполнять свои функции, и в процессе его активности в клетке. В живых организмах часто несколько молекул формируют сложные комплексы. В качестве примера можно привести фотосинтетическое объединение.
Назначение соединений
Белки считаются важной составляющей питания человека и животных в связи с тем, что в их организмах все необходимые аминокислоты синтезироваться не могут. Часть их должна поступать вместе с белковой пищей. Основными источниками соединений выступают мясо, орехи, молоко, рыба, зерновые. В меньшей степени протеины присутствуют в овощах, грибах и ягодах. При пищеварении посредством ферментов потребленные белки подвергаются разрушению до аминокислот. Они уже используются в биосинтезе собственных протеинов в организме либо подвергаются распаду дальше - для получения энергии.

Историческая справка
Последовательность структуры белка инсулина была определена впервые Фредериеом Сенгером. За свою работу он получил Нобелевскую премию в 1958 году. Сенгер использовал метод секвенирования. С помощью дифракции рентгеновского излучения впоследствии были получены трехмерные структуры миоглобина и гемоглобина (в конце 1950 гг.). Работы проводили Джон Кендрю и Макс Перуц.
Структура молекулы белка
Она включает в себя линейные полимеры. Они, в свою очередь, состоят из остатков альфа-аминокислот, являющихся мономерами. Кроме того, структура белка может включать компоненты, имеющие неаминокислотную природу, и аминокислотные остатки модифицированного типа. При обозначении компонентов применяются 1- либо 3-буквенные сокращения. Соединение, в состав которого входит от двух до нескольких десятков остатков, именуется часто как "полипептид". В результате взаимодействия альфа-карбоксильной группы одной аминокислоты с альфа-аминогруппой другой появляются (в процессе формирования структуры белка) связи. В соединении выделяют С- и N- концы, в зависимости от того, какая группа аминокислотного остатка является свободной: -СООН либо -NH 2 . В процессе синтеза белка на рибосоме в качестве первого концевого выступает, как правило, остаток метионина; присоединение последующих осуществляется к С-концу предыдущих.

Уровни организации
Они были предложены Линдрем-Лангом. Несмотря на то что данное деление считается несколько устаревшим, им все еще пользуются. Было предложено выделять четыре уровня организации соединений. Первичная структура молекулы белка определяется генетическим кодом и особенностями гена. Для более высоких уровней характерно формирование в ходе сворачивания протеина. Пространственная структура белка определяется в целом аминокислотной цепью. Тем не менее она достаточно лабильна. На нее могут оказывать влияние внешние факторы. В связи с этим более корректно говорить о конформации соединения, наиболее выгодной и предпочтительной энергетически.
1 уровень
Он представлен последовательностью аминокислотных остатков полипептидной цепи. Как правило, его описывают с использованием одно- либо трехбуквенных обозначений. Первичная структура белков отличается устойчивыми сочетаниями аминокислотных остатков. Они выполняют определенные задачи. Такие "консервативные мотивы" остаются сохраненными в ходе видовой эволюции. По ним достаточно часто можно предсказывать задачу неизвестного протеина. Оценивая степень сходства (гомологии) в аминокислотных цепях от различных организмов, можно определять эволюционное расстояние, образующееся между таксонами, которые составляют эти организмы. Первичная структура белков определяется методом секвенирования либо по исходному комплексу его мРНК с использованием таблицы генетического кода.

Локальное упорядочивание участка цепи
Это следующий уровень организации - вторичная структура белков. Существует несколько ее типов. Локальное упорядочивание участка цепи полипептида стабилизируется водородными связями. Наиболее популярными типами считаются:

Пространственное строение
Третичная структура белков включает в себя элементы предыдущего уровня. Они стабилизируются разными типами взаимодействий. Важнейшее значение при этом имеют гидрофобные связи. В стабилизации участвуют:
- Ковалентные взаимодействия.
- Ионные связи, формирующиеся между боковыми аминокислотными группами, имеющими противоположные заряды.
- Водородные взаимодействия.
- Гидрофобные связи. В процессе взаимодействия с окружающими элементами Н 2 О происходит сворачивание протеина так, чтобы боковые неполярные аминокислотные группы оказывались изолированными от водного раствора. Гидрофильные группы (полярные) оказываются на поверхности молекулы.
Третичная структура белков определяется методами магнитного (ядерного) резонанса, некоторыми видами микроскопии и прочими способами.
Принцип укладки
Исследования показали, что между 2 и 3 уровнями удобно выделить еще один. Его именуют "архитектурой", "мотивом укладки". Он определяется взаиморасположением компонентов вторичной структуры (бета-тяжей и альфа-спиралей) в границах компактной глобулы - белкового домена. Он может существовать самостоятельно либо быть включенным в состав более крупного протеина вместе с прочими аналогичными. Установлено, что мотивы укладки достаточно консервативны. Они встречаются в протеинах, не обладающих ни эволюционными, ни функциональными связями. Определение архитектуры лежит в основе рациональной (физической) классификации.

Доменная организация
При взаимном расположении нескольких цепей полипептидов в составе одного протеинового комплекса формируется четвертичная структура белков. Элементы, входящие в ее состав, образуются по отдельности на рибосомах. Только по завершении синтеза начинает образовываться данная структура белка. Она может содержать как различающиеся, так и идентичные полипептидные цепи. Четвертичная структура белков стабилизируется за счет тех же взаимодействий, что и на предыдущем уровне. Некоторые комплексы могут включать в себя несколько десятков протеинов.
Структура белка: защитные задачи
Полипептиды цитоскелета, выступая в некотором роде в качестве арматуры, придают многим органоидам форму, участвуют в ее изменении. Структурные протеины обеспечивают защиту организма. К примеру, таким белком является коллаген. Он формирует основу в межклеточном веществе соединительных тканей. Также защитной функцией обладает кератин. Он составляет основу рогов, перьев, волос и прочих производных эпидермиса. При связывании белками токсинов во многих случаях происходит детоксикация последних. Так выполняется задача по химической защите организма. Особенно важную роль в процессе обезвреживания токсинов в человеческом организме играют печеночные ферменты. Они способны расщеплять яды или переводить их в растворимую форму. Это способствует более быстрой транспортировке их из организма. Белки, присутствующие в крови и прочих биологических жидкостях, обеспечивают иммунную защиту, вызывая реакцию как на атаку патогенов, так и на повреждение. Иммуноглобулины (антитела и компоненты системы комплемента) способны нейтрализовывать бактерии, чужеродные протеины и вирусы.
Механизм регуляции
Белковые молекулы, не выступающие ни в качестве источника энергии, ни как строительный материал, контролируют многие внутриклеточные процессы. Так, за счет них осуществляется регулирование трансляции, транскрипции, слайсинга, деятельность прочих полипептидов. Механизм регуляции основывается на ферментативной активности или проявляется благодаря специфичному связыванию с прочими молекулами. К примеру, факторы транскрипции, полипептиды-активаторы и протеины- репрессоры способны контролировать интенсивность генной транскрипции. При этом они взаимодействуют с регуляторными последовательностями генов. Важнейшая роль в контроле над течением внутриклеточных процессов отводится протеинфосфатазам и протеинкиназам. Эти ферменты запускают либо подавляют активность прочих белков посредством присоединения или отщепления от них фосфатных групп.

Сигнальная задача
Ее часто объединяют с регуляторной функцией. Это связано с тем, что многие внутриклеточные, как и внеклеточные, полипептиды могут передавать сигналы. Такой способностью обладают факторы роста, цитокины, гормоны и прочие соединения. Стероиды транспортируются по крови. Взаимодействие гормона с рецептором выступает в качестве сигнала, за счет которого запускается ответная реакция клетки. Стероиды контролируют содержание соединений в крови и клетках, размножение, рост и прочие процессы. В качестве примера можно привести инсулин. Он регулирует уровень глюкозы. Взаимодействие клеток осуществляется посредством сигнальных белковых соединений, передаваемых по межклеточному веществу.
Транспорт элементов
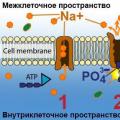
Растворимые протеины, участвующие в перемещении малых молекул, имеют высокое сродство к субстрату, присутствующему в повышенной концентрации. Они обладают также способностью к легкому его высвобождению в областях с низким его содержанием. В качестве примера можно привести транспортный белок гемоглобин. Он перемещает из легких кислород к прочим тканям, а от них - переносит углекислый газ. В транспортировке малых молекул через стенки клетки, изменяя их, участвуют и некоторые мембранные белки. Липидный слой цитоплазмы обладает водонепроницаемостью. Благодаря этому предотвращается диффузия заряженных или полярных молекул. Мембранные транспортные соединения принято разделять на переносчиков и каналы.
Резервные соединения
Эти белки формируют так называемые запасы. Они накапливаются, например, в семенах растений, животных яйцеклетках. Такие белки выступают в качестве резервного источника вещества и энергии. Некоторые соединения используются организмом как аминокислотный резервуар. Они, в свою очередь, являются предшественниками активных веществ, участвующих в регулировании метаболизма.
Клеточные рецепторы
Такие белки могут располагаться как непосредственно в цитоплазме, так и встраиваться в стенку. Одной своей частью соединение принимает сигнал. В качестве него, как правило, выступает химическое вещество, а в ряде случаев - механическое воздействие (растяжение, к примеру), свет и прочие стимулы. В процессе воздействия сигнала на определенный фрагмент молекулы - полипептид-рецептор - начинаются ее конформационные изменения. Они провоцируют смену конформации остальной части, выполняющей передачу стимула на прочие компоненты клетки. Отправка сигнала может осуществляться разными способами. Одни рецепторы способны катализировать химическую реакцию, вторые - выступают в качестве ионных каналов, закрывающихся либо открывающихся под воздействием стимула. Некоторые соединения специфически связывают молекулы-посредники внутри клетки.
Моторные полипептиды
Существует целый класс белков, обеспечивающих движения организма. Моторные белки участвуют в сокращении мышц, перемещении клеток, активности жгутиков и ресничек. За счет них также выполняется направленные и активный транспорт. Кинезины и динеины осуществляют перенос молекул по ходу микротрубочек с использованием в качестве энергетического источника гидролиза АТФ. Вторые перемещают органоиды и прочие элементы по направлению к центросоме из периферических клеточных участков. Кинезины движутся в обратном направлении. Динеины, кроме того, отвечают за активность жгутиков и ресничек.