Скорость химической реакции
Тема «Скорость химической
реакции», пожалуй, наиболее сложная и
противоречивая в школьной программе. Это связано
со сложностью самой химической кинетики –
одного из разделов физической химии.
Неоднозначно уже само определение понятия
«скорость химической реакции» (см., например,
статью Л.С.Гузея в газете «Химия», 2001, № 28,
с. 12). Еще больше проблем возникает при попытке
применить закон действующих масс для скорости
реакции к любым химическим системам, ведь круг
объектов, для которых возможно количественное
описание кинетических процессов в рамках
школьной программы, очень узок. Хотелось бы особо
отметить некорректность использования закона
действующих масс для скорости химической
реакции при химическом равновесии.
В то же время вообще отказаться от рассмотрения
этой темы в школе было бы неверным. Представления
о скорости химической реакции очень важны при
изучении многих природных и технологических
процессов, без них невозможно говорить о
катализе и катализаторах, в том числе и о
ферментах. Хотя при обсуждении превращений
веществ используются в основном качественные
представления о скорости химической реакции,
введение простейших количественных соотношений
все же желательно, особенно для элементарных
реакций.
В публикуемой статье достаточно подробно
рассматриваются вопросы химической кинетики,
которые можно обсуждать на школьных уроках
химии. Исключение из курса школьной химии
спорных и противоречивых моментов этой темы
особенно важно для тех учащихся, кто собирается
продолжить свое химическое образование в вузе.
Ведь полученные в школе знания нередко вступают
в противоречие с научной реальностью.
Химические реакции могут существенно различаться по времени протекания. Смесь водорода и кислорода при комнатной температуре может долгое время оставаться практически без изменений, однако при ударе или поджигании произойдет взрыв. Железная пластина медленно ржавеет, а кусочек белого фосфора самовоспламеняется на воздухе. Важно знать, насколько быстро протекает та или иная реакция, чтобы иметь возможность контролировать ее ход.
Основные понятия
Количественной характеристикой того, насколько быстро протекает данная реакция, является скорость химической реакции, т. е. скорость расходования реагентов или скорость появления продуктов. При этом безразлично, о каком из участвующих в реакции веществе идет речь, поскольку все они связаны между собой через уравнение реакции. По изменению количества одного из веществ можно судить о соответствующих изменениях количеств всех остальных.
Скоростью химической реакции () называют изменение количества вещества реагента или продукта () за единицу времени () в единице объема (V ):
= /(V ).
Скорость реакции в данном случае обычно выражается в моль/(л с).
Приведенное выражение относится к гомогенным химическим реакциям, протекающим в однородной среде, например между газами или в растворе:
2SO 2 + O 2 = 2SO 3 ,
BаСl 2 + Н 2 SO 4 = ВаSО 4 + 2НСl.
Гетерогенные химические реакции идут на поверхности соприкосновения твердого вещества и газа, твердого вещества и жидкости и т.п. К гетерогенным реакциям относятся, например, реакции металлов с кислотами:
Fе + 2НСl = FeСl 2 + Н 2 .
В этом случае скоростью реакции называют изменение количества вещества реагента или продукта () за единицу времени () на единице поверхности (S):
= /(S ).
Скорость гетерогенной реакции выражается в моль/(м 2 с).
Чтобы управлять химическими реакциями, важно не только уметь определять их скорости, но и выяснить, какие условия оказывают на них влияние. Раздел химии, изучающий скорость химических реакций и влияние на нее различных факторов, называется химической кинетикой .
Частота соударений реагирующих частиц
Важнейший фактор, определяющий скорость химической реакции, – концентрация .
При повышении концентрации реагирующих веществ скорость реакции, как правило, возрастает. Для того чтобы вступить в реакцию, две химические частицы должны сблизиться, поэтому скорость реакции зависит от числа столкновений между ними. Увеличение числа частиц в данном объеме приводит к более частым столкновениям и к возрастанию скорости реакции.
Для гомогенных реакций повышение концентрации одного или нескольких реагирующих веществ приведет к увеличению скорости реакции. При понижении концентрации наблюдается противоположный эффект. Концентрация веществ в растворе может быть изменена путем добавления или удаления из сферы реакции реагирующих веществ или растворителя. В газах концентрация одного из веществ может быть увеличена путем введения дополнительного количества этого вещества в реакционную смесь. Концентрации всех газообразных веществ можно увеличить одновременно, уменьшая объем, занимаемый смесью. При этом скорость реакции возрастет. Увеличение объема приводит к обратному результату.
Скорость гетерогенных реакций зависит от площади поверхности соприкосновения веществ , т.е. от степени измельчения веществ, полноты смешивания реагентов, а также от состояния кристаллических структур твердых тел. Любые нарушения в кристаллической структуре вызывают увеличение реакционной способности твердых тел, т.к. для разрушения прочной кристаллической структуры требуется дополнительная энергия.
Рассмотрим горение древесины. Целое полено горит на воздухе сравнительно медленно. Если увеличить поверхность соприкосновения дерева с воздухом, расколов полено на щепки, скорость горения увеличится. Вместе с тем древесина горит в чистом кислороде значительно быстрее, чем на воздухе, который содержит лишь около 20% кислорода.
Для протекания химической реакции должно произойти столкновение частиц – атомов, молекул или ионов. В результате столкновений происходит перегруппировка атомов и возникают новые химические связи, что приводит к образованию новых веществ. Вероятность столкновения двух частиц достаточно высока, вероятность одновременного столкновения трех частиц существенно меньше. Одновременное столкновение четырех частиц чрезвычайно маловероятно. Поэтому большинство реакций протекает в несколько стадий, на каждой из которых происходит взаимодействие не более трех частиц.
Реакция окисления бромоводорода протекает с заметной скоростью при 400–600 °С:
4НВr + O 2 = 2Н 2 О + 2Вr 2 .
В соответствии с уравнением реакции одновременно должно столкнуться пять молекул. Однако вероятность такого события практически равна нулю. Более того, экспериментальные исследования показали, что повышение концентрации – либо кислорода, либо бромоводорода – увеличивает скорость реакции в одно и то же число раз. И это при том, что на каждую молекулу кислорода расходуется четыре молекулы бромоводорода.
Детальное рассмотрение данного процесса показывает, что он протекает в несколько стадий:
1) НBr + О 2 = НООВr (медленная реакция);
2) НООВr + НВr = 2НОВr (быстрая реакция);
3) НОВr + НВr = Н 2 О + Вr 2 (быстрая реакция).
Приведенные реакции, так называемые элементарные реакции , отражают механизм реакции окисления бромоводорода кислородом. Важно отметить, что в каждой из промежуточных реакций участвует только по две молекулы. Сложение первых двух уравнений и удвоенного третьего дает суммарное уравнение реакции. Общая же скорость реакции определяется наиболее медленной промежуточной реакцией, в которой взаимодействуют одна молекула бромоводорода и одна молекула кислорода.
Скорость элементарных реакций прямо пропорциональна произведению молярных концентраций с (с – это количество вещества в единице объема, с = /V ) реагентов, взятых в степенях, равных их стехиометрическим коэффициентам (закон действующих масс для скорости химической реакции). Это справедливо лишь для уравнений реакций, отражающих механизмы реальных химических процессов, когда стехиометрические коэффициенты перед формулами реагентов соответствуют числу взаимодействующих частиц.
По числу взаимодействующих в реакции молекул различают реакции мономолекулярные, бимолекулярные и тримолекулярные. Например, диссоциация молекулярного йода на атомы: I 2 = 2I – мономолекулярная реакция.
Взаимодействие йода с водородом: I 2 + Н 2 = 2HI – бимолекулярная реакция. Закон действующих масс для химических реакций разной молекулярности записывается по-разному.
Мономолекулярные реакции:
А = В + С,
= kc A ,
где k – константа скорости реакции.
Бимолекулярные реакции:
= kc A c В.
Тримолекулярные реакции:
= kc 2 A c В.
Энергия активации
Столкновение химических частиц приводит к химическому взаимодействию лишь в том случае, если сталкивающиеся частицы обладают энергией, превышающей некоторую определенную величину. Рассмотрим взаимодействие газообразных веществ, состоящих из молекул А 2 и В 2:
А 2 + В 2 = 2АВ.
В ходе химической реакции происходит перегруппировка атомов, сопровождающаяся разрывом химических связей в исходных веществах и образованием связей в продуктах реакции. При столкновении реагирующих молекул сначала образуется так называемый активированный комплекс , в котором происходит перераспределение электронной плотности, и лишь потом получается конечный продукт реакции:

Энергию, необходимую для перехода веществ в состояние активированного комплекса, называют энергией активации .
Активность химических веществ проявляется в низкой энергии активации реакций с их участием. Чем ниже энергия активации, тем выше скорость реакции. Например, в реакциях между катионами и анионами энергия активации очень мала, поэтому такие реакции протекают почти мгновенно. Если энергия активации велика, то очень малая часть соударений приводит к образованию новых веществ. Так, скорость реакции между водородом и кислородом при комнатной температуре практически равна нулю.
Итак, на скорость реакции оказывает влияние природа реагирующих веществ . Рассмотрим для примера реакции металлов с кислотами. Если опустить в пробирки с разбавленной серной кислотой одинаковые кусочки меди, цинка, магния и железа, можно увидеть, что интенсивность выделения пузырьков газообразного водорода, характеризующая скорость протекания реакции, для этих металлов существенно различается. В пробирке с магнием наблюдается бурное выделение водорода, в пробирке с цинком пузырьки газа выделяются несколько спокойнее. Еще медленнее протекает реакция в пробирке с железом (рис.). Медь вообще не вступает в реакцию с разбавленной серной кислотой. Таким образом, скорость реакции зависит от активности металла.
При замене серной кислоты (сильной кислоты) на уксусную (слабую кислоту) скорость реакции во всех случаях существенно замедляется. Можно сделать вывод, что на скорость реакции металла с кислотой влияет природа обоих реагентов – как металла, так и кислоты.
Повышение температуры приводит к увеличению кинетической энергии химических частиц, т.е. увеличивает число частиц, имеющих энергию выше энергии активации. При повышении температуры число столкновений частиц также увеличивается, что в некоторой степени увеличивает скорость реакции. Однако повышение эффективности столкновений за счет увеличения кинетической энергии оказывает большее влияние на скорость реакции, чем увеличение числа столкновений.
При повышении температуры на десять градусов скорость увеличивается в число раз, равное температурному коэффициенту скорости :
= T +10 /T .
При повышении температуры от T
до T
"
отношение скоростей реакций T
" и T
равно
температурному коэффициенту скорости в степени (T
"
– T
)/10:
T " /T = (T "–T )/10.
Для многих гомогенных реакций температурный коэффициент скорости равен 24 (правило Вант-Гоффа). Зависимость скорости реакции от температуры можно проследить на примере взаимодействия оксида меди(II) с разбавленной серной кислотой. При комнатной температуре реакция протекает очень медленно. При нагревании реакционная смесь быстро окрашивается в голубой цвет за счет образования сульфата меди(II):
СuО + Н 2 SО 4 = СuSO 4 + Н 2 О.
Катализаторы и ингибиторы
Многие реакции можно ускорить или замедлить путем введения некоторых веществ. Добавляемые вещества не участвуют в реакции и не расходуются в ходе ее протекания, но оказывают существенное влияние на скорость реакции. Эти вещества изменяют механизм реакции (в том числе состав активированного комплекса) и понижают энергию активации, что обеспечивает ускорение химических реакций. Вещества – ускорители реакций называют катализаторами , а само явление такого ускорения реакции – катализом .
Многие реакции в отсутствие катализаторов протекают очень медленно или не протекают совсем. Одной из таких реакций является разложение пероксида водорода:
2Н 2 О 2 = 2Н 2 О + О 2 .
Если опустить в сосуд с водным раствором пероксида водорода кусочек твердого диоксида марганца, то начнется бурное выделение кислорода. После удаления диоксида марганца реакция практически прекращается. Путем взвешивания нетрудно убедиться, что диоксид марганца в данном процессе не расходуется – он лишь катализирует реакцию.
В зависимости от того, в одинаковых или различных агрегатных состояниях находится катализатор и реагирующие вещества, различают гомогенный и гетерогенный катализ.
При гомогенном катализе катализатор может ускорить реакцию путем образования промежуточных веществ за счет взаимодействия с одним из исходных реагентов. Например:
![]()
При гетерогенном катализе химическая реакция обычно протекает на поверхности катализатора:
![]()
Катализаторы широко распространены в природе. Практически все превращения веществ в живых организмах протекают с участием органических катализаторов – ферментов.
Катализаторы используют в химическом производстве для ускорения тех или иных процессов. Кроме них применяют также вещества, замедляющие химические реакции, – ингибиторы . С помощью ингибиторов, в частности, защищают металлы от коррозии.
Факторы, влияющие на скорость химической реакции
| Увеличивают скорость | Уменьшают скорость |
|---|---|
| Наличие химически активных реагентов | Наличие химически неактивных реагентов |
| Повышение концентрации реагентов | Понижение концентрации реагентов |
| Увеличение поверхности твердых и жидких реагентов | Уменьшение поверхности твердых и жидких реагентов |
| Повышение температуры | Понижение температуры |
| Присутствие катализатора | Присутствие ингибитора |
ЗАДАНИЯ
1. Дайте определение скорости химической реакции. Напишите выражение кинетического закона действующих масс для следующих реакций:
а) 2С (тв.) + О 2 (г.) = 2СО (г.);
б) 2НI (г.) = Н 2 (г.) + I 2 (г.).
2. От чего зависит скорость химической реакции? Приведите математическое выражение зависимости скорости химической реакции от температуры.
3. Укажите, как влияет на скорость реакции (при постоянном объеме):
а) увеличение концентрации реагентов;
б) измельчение твердого реагента;
в) понижение температуры;
г) введение катализатора;
д) уменьшение концентрации реагентов;
е) повышение температуры;
ж) введение ингибитора;
з) уменьшение концентрации продуктов.
4. Рассчитайте скорость химической реакции
СО (г.) + Н 2 О (г.) = СО 2 (г.) + Н 2 (г.)
в сосуде емкостью 1 л, если через 1 мин 30 с после ее начала количество вещества водорода было 0,32 моль, а через 2 мин 10 с стало 0,44 моль. Как повлияет на скорость реакции увеличение концентрации СО?
5. В результате одной реакции за определенный промежуток времени образовалось 6,4 г йодоводорода, а в другой реакции в тех же условиях – 6,4 г диоксида серы. Сравните скорости этих реакций. Как изменятся скорости этих реакций при повышении температуры?
6. Определите скорость реакции
СО (г.) + Сl 2 (г.) = СОCl 2 (г.),
если через 20 с после начала реакции исходное
количество вещества оксида углерода(II)
уменьшилось c 6 моль в 3 раза (объем реактора равен
100 л). Как изменится скорость реакции, если вместо
хлора использовать менее активный бром? Как
изменится скорость реакции при введении
а) катализатора; б) ингибитора?
7. В каком случае реакция
СaО (тв.) + СО 2 (г.) = СaCO 3 (тв.)
протекает быстрее: при использовании крупных
кусков или порошка оксида кальция? Рассчитайте:
а) количество вещества; б) массу карбоната
кальция, образовавшегося за 10 с, если скорость
реакции составляет 0,1 моль/(л с), объем реактора
равен 1 л.
8. Взаимодействие образца магния с хлороводородной кислотой НСl позволяет получить 0,02 моль хлорида магния через 30 с после начала реакции. Определите, за какое время можно получить 0,06 моль хлорида магния.
Е) от 70 до 40 °С скорость реакции уменьшилась в 8
раз;
ж) от 60 до 40 °С скорость реакции уменьшилась в
6,25 раза;
з) от 40 до 10 °С скорость реакции уменьшилась в 27
раз.
11. Владелец автомашины покрасил ее новой краской, а затем обнаружил, что согласно инструкции она должна сохнуть 3 ч при 105 °С. За какое время высохнет краска при 25 °С, если температурный коэффициент реакции полимеризации, лежащей в основе этого процесса, равен: а) 2; б) 3; в) 4?
ОТВЕТЫ НА ЗАДАНИЯ
1. а) = kc (О 2); б) = kc (HI) 2 .
2. T +10 = T .
3. Скорость реакции увеличивается в случаях а, б, г, е; уменьшается – в, д, ж; не изменяется – з.
4. 0,003 моль/(л с). При увеличении концентрации СО скорость реакции возрастает.
5. Скорость первой реакции в 2 раза ниже.
6. 0,002 моль/(л с).
7. а) 1 моль; б) 100 г.
9. Увеличатся в 2 раза скорости реакций д, ж, з; в 4 раза – а, б, е; в 8 раз – в, г.
10. Температурный коэффициент:
2 для реакций б, е; = 2,5 – в, ж; = 3 – д, з; = 3,5 – а, г.
а) 768 ч (32 сут, т. е. более 1 месяца);
б) 19 683 ч (820 сут, т. е. более 2 лет);
в) 196 608 ч (8192 сут, т. е. 22 года).
Темы кодификатора ЕГЭ: Скорость реакции. Ее зависимость от разных факторов.
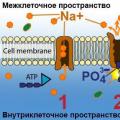
Скорость химической реакции показывает, как быстро происходит та или иная реакция. Взаимодействие происходит при столкновении частиц в пространстве. При этом реакция происходит не при каждом столкновении, а только когда частица обладают соответствующей энергией.
Скорость реакции – количество элементарных соударений взаимодействующих частиц, заканчивающихся химическим превращением, за единицу времени.
Определение скорости химической реакции связано с условиями ее проведения. Если реакция гомогенная – т.е. продукты и реагенты находятся в одной фазе – то скорость химической реакции определяется, как изменение вещества в единицу времени:
υ = ΔC / Δt.
Если реагенты, или продукты находятся в разных фазах, и столкновение частиц происходит только на границе раздела фаз, то реакция называется гетерогенной , и скорость ее определяется изменением количества вещества в единицу времени на единицу реакционной поверхности:
υ = Δν / (S·Δt).
Как заставить частицы чаще сталкиваться, т.е. как увеличить скорость химической реакции ?
1. Самый простой способ – повысить температуру . Как вам, должно быть, известно из курса физики, температура – это мера средней кинетической энергии движения частиц вещества. Если мы повышаем температуру, то частицы любого вещества начинают двигаться быстрее, а следовательно, сталкиваться чаще.
Однако при повышении температуры скорость химических реакций увеличивается в основном благодаря тому, что увеличивается число эффективных соударений. При повышении температуры резко увеличивается число активных частиц, которые могут преодолеть энергетичекий барьер реакции. Если понижаем температуру – частицы начинают двигаться медленнее, число активных частиц уменьшается, и количество эффективных соударений в секунду уменьшается. Таким образом, при повышении температуры скорость химической реакции повышается, а при понижении температуры — уменьшается .
Обратите внимание! Это правило работает одинаково для всех химических реакций (в том числе для экзотермических и эндотермических). Скорость реакции не зависит от теплового эффекта. Скорость экзотермических реакций при повышении температуры возрастает, а при понижении температуры – уменьшается. Скорость эндотермических реакций также возрастает при повышении температуры, и уменьшается при понижении температуры.
Более того, еще в XIX веке голландский физик Вант-Гофф экспериментально установил, что большинство реакций примерно одинаково увеличивают скорость (примерно в 2-4 раза) при повышении температуры на 10 о С. Правило Вант-Гоффа звучит так: повышение температуры на 10 о С приводит к увеличению скорости химической реакции в 2-4 раза (эту величину называют температурный коэффициент скорости химической реакции γ). Точное значение температурного коэффициента определяется для каждой реакции.
Здесь v 2 — скорость реакции при температуре T 2 , v 1 — скорость реакции при температуре T 1 , γ — температурный коэффициент скорости реакции, коэффинциент Вант-Гоффа.
В некоторых ситуациях повысить скорость реакции с помощью температуры не всегда удается, т.к. некоторые вещества разлагаются при повышении температуры, некоторые вещества или арстворители испаряются при повышенной температуре и т.д., т.е. нарушаются условия проведения процесса.
2. Концентрация. Также повысить число эффективных соударений можно, изменив концентрацию реагирующих веществ . как правило, используется для газов и жидкостей, т.к. в газах и жидкостях частицы быстро двигаются и активно перемешиваются. Чем больше концентрация реагирующих веществ (жидкостей, газов), тем больше число эффективных соударений, и тем выше скорость химической реакции.
На основании большого числа экспериментов в 1867 году в работах норвежских ученых П. Гульденберга и П. Вааге и, независимо от них, в 1865 году русским ученым Н.И. Бекетовым был выведен основной закон химической кинетики, устанавливающий зависимость скорости химической реакции от концентрации реагирующих веществ:
Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях, равных их коэффициентам в уравнении химической реакции.
Для химической реакции вида: aA + bB = cC + dD закон действующих масс записывается так:
![]()
здесь v — скорость химической реакции,
C A и C B — концентрации веществ А и В, соответственно, моль/л
k – коэффициент пропорциональности, константа скорости реакции.
Например , для реакции образования аммиака:
N 2 + 3H 2 ↔ 2NH 3
закон действующих масс выглядит так:
![]() Константа скорости реакции показывает, с какой скоростью будут реагировать вещества, если их концентрации равны 1 моль/л, или их произведение равно 1. Константа скорости химической реакции зависит от температуры и не зависит от концентрации реагирующих веществ.
Константа скорости реакции показывает, с какой скоростью будут реагировать вещества, если их концентрации равны 1 моль/л, или их произведение равно 1. Константа скорости химической реакции зависит от температуры и не зависит от концентрации реагирующих веществ.
В законе действующих масс не учитываются концентрации твердых веществ, т.к. они реагируют, как правило, на поверхности, и количество реагирующих частиц на единицу поверхности при этом не меняется.
В большинстве случаев химическая реакция осстоит из несольких простых этапов, в таком случае уравнение химической реакции показывает лишь суммарное или итоговое уравнение происходящих процессов. При этом скорость химической реакции сложным образом зависит (или не зависит) от концентрации реагирующих веществ, полупродуктов или катализатора, поэтому точная форма кинетического уравнения определяется экспериментально, или на основании анализа предполагаемого механизма реакции. Как правило, скорость сложной химической реакции определяется скоростью его самого медленного этапа (лимитирующей стадии ).
3. Давление. Для газов концентрация напрямую зависит от давления . При повышении давления повышается концентрация газов. Математическое выражение этой зависимости (для идеального газа) — уравнение Менделеева-Клапейрона:
pV = νRT
Таким образом, если среди реагентов есть газообразное вещество, то при повышении давления скорость химической реакции увеличивается, при понижении давления — уменьшается .
Например. Как изменится скорость реакции сплавления извести с оксидом кремния:
CaCO 3 + SiO 2 ↔ CaSiO 3 + CO 2
при повышении давления?
Правильным ответом будет – никак, т.к. среди реагентов нет газов, а карбонат кальция – твердая соль, нерастворимая в воде, оксид кремния – твердое вещество. Газом будет продукт – углекислый газ. Но продукты не влияют на скорость прямой реакции.
Еще один способ увеличить скорость химической реакции – направить ее по другому пути, заменив прямое взаимодействие, например, веществ А и В серией последовательных реакций с третьим веществом К, которые требуют гораздо меньших затрат энергии (имеют более низкий активационный энергетический барьер) и протекают при данных условиях быстрее, чем прямая реакция. Это третье вещество называют катализатором .

– это химические вещества, участвующие в химической реакции, изменяющие ее скорость и направление, но не расходующиеся в ходе реакции (по окончании реакции не изменяющиеся ни по количеству, ни по составу). Примерный механизм работы катализатора для реакции вида А + В можно изобрать так:
A + K = AK
AK + B = AB + K
Процесс изменения скорости реакции при взаимодействии с катализатором называют катализом . Катализаторы широко применяют в промышленности, когда необходимо увеличить скорость реакции, либо направить ее по определенному пути.
По фазовому состоянию катализатора различают гомогенный и гетерогенный катализ.
Гомогенный катализ – это когда реагирующие вещества и катализатор находятся в одной фазе (газ, раствор). Типичные гомогенные катализаторы – кислоты и основания. органические амины и др.
Гетерогенный катализ – это когда реагирующие вещества и катализатор находятся в разных фазах. Как правило, гетерогенные катализаторы – твердые вещества. Т.к. взаимодействие в таких катализаторах идет только на поверхности вещества, важным требованием для катализаторов является большая площадь поверхности. Гетерогенные катализаторы отличает высокая пористость, которая увеличивает площадь поверхности катализатора. Так, суммарная площадь поверхности некоторых катализаторов иногда достигает 500 квадратных метров на 1 г катализатора. Большая площадь и пористость обеспечивают эффективное взаимодействие с реагентами. К гетерогенным катализаторам относятся металлы, цеолиты - кристаллические минералы группы алюмосиликатов (соединений кремния и алюминия), и другие.

Пример гетерогенного катализа – синтез аммиака :
N 2 + 3H 2 ↔ 2NH 3
В качестве катализатора используется пористое железо с примесями Al 2 O 3 и K 2 O.
Сам катализатор не расходуется в ходе химической реакции, но на поверхности катализатора накапливаются другие вещества, связывающие активные центры катализатора и блокирующие его работу (каталитические яды ). Их необходимо регулярно удалять, путем регенерации катализатора.
В биохимических реакция очень эффективными оказываются катализаторы – ферменты . Ферментативные катализаторы действуют высокоэффективно и избирательно, с избарительностю 100%. К сожалению, ферменты очень чувствительны к повышению температуры, кислотности среды и другим факторам, поэтому есть ряд ограничений для реализации в промышленных масштабах процессов с ферментативным катализом.
Катализаторы не стоит путать с инициаторами процесса и ингибиторами . Например , для инициирования радикальной реакции хлорирования метана необходимо облучение ультрафиолетом. Это не катализатор. Некоторые радикальные реакции инициируются пероксидными радикалами. Это также не катализаторы.
Ингибиторы – это вещества, которые замедляют химическую реакцию. Ингибиторы могут расходоваться и участвовать в химической реакции. При этом ингибиторы не являются катализаторами наоброт. Обратный катализ в принципе невозможен – реакция в любом случае будет пытаться идти по наиболее быстрому пути.
5. Площадь соприкосновения реагирующих веществ. Для гетерогенных реакций одним из способов увеличить число эффективных соударений является увеличение площади реакционной поверхности . Чем больше площадь поверхности контакта реагирующих фаз, тем больше скорость гетерогенной химической реакции. Порошковый цинк гораздо быстрее растворяется в кислоте, чем гранулированный цинк такой же массы.
В промышленности для увеличения площади контактирующей поверхности реагирующих веществ используют метод кипящего слоя . Например , при производстве серной кислоты методом кипящег ослоя производят обжиг колчедана.
6. Природа реагирующих веществ . На скорость химических реакций при прочих равных условиях также оказывают влияние химические свойства, т.е. природа реагирующих веществ. Менее активные вещества будут имеют более высокий активационный барьер, и вступают в реакции медленнее, чем более активные вещества. Более активные вещества имеют более низкую энергию активации, и значительно легче и чаще вступают в химические реакции.
При небольших значениях энергии активации (менее 40 кДж/моль) реакция проходит очень быстро и легко. Значительная часть столкновений между частицами заканчивается химическим превращением. Например, реакции ионного обмена происходят при обычных условиях очень быстро.
При высоких значениях энергии активации (более 120 кДж/моль) лишь незначительное число столкновений заканчивается химическим превращением. Скорость таких реакций пренебрежимо мала. Например, азот с кислородом практически не взаимодействует при нормальных условиях.
При средних значениях энергии активации (от 40 до 120 кДж/моль) скорость реакции будет средней. Такие реакции также идут при обычных условиях, но не очень быстро, так, что их можно наблюдать невооруженным глазом. К таким реакциям относятся взаимодействие натрия с водой, взаимодействие железа с соляной кислотой и др.
Вещества, стабильные при нормальных условиях, как правило, имеют высокие значения энергии активации.
ОПРЕДЕЛЕНИЕ
Химическая кинетика – учение о скоростях и механизмах химических реакций.
Изучение скоростей протекания реакций, получение данных о факторах, влияющих на скорость химической реакции, а также изучение механизмов химических реакций осуществляют экспериментально.
ОПРЕДЕЛЕНИЕ
Скорость химической реакции – изменение концентрации одного из реагирующих веществ или продуктов реакции в единицу времени при неизменном объеме системы.
Скорость гомогенной и гетерогенной реакций определяются различно.
Определение меры скорости химической реакции можно записать в математической форме. Пусть – скорость химической реакции в гомогенной системе, n B – число моле какого-либо из получающихся при реакции веществ, V – объем системы, – время. Тогда в пределе:
Это уравнение можно упростить – отношение количества вещества к объему представляет собой молярную концентрацию вещества n B /V = c B , откуда dn B / V = dc B и окончательно:
На практике измеряют концентрации одного или нескольких веществ в определенные промежутки времени. Концентрации исходных веществ со временем уменьшаются, а концентрации продуктов – увеличиваются (рис. 1).

Рис. 1. Изменение концентрации исходного вещества (а) и продукта реакции (б) со временем
Факторы, влияющие на скорость химической реакции
Факторами, оказывающими влияние на скорость химической реакции, являются: природа реагирующих веществ, их концентрации, температура, присутствие в системе катализаторов, давление и объем (в газовой фазе).
С влиянием концентрации на скорость химической реакции связан основной закон химической кинетики – закон действующих масс (ЗДМ): скорость химической реакции прямопропорциональна произведению концентраций реагирующих веществ, возведенных в степени их стехиометрических коэффициентов. ЗДМ не учитывает концентрацию веществ в твердой фазе в гетерогенных системах.
Для реакции mA +nB = pC +qD математическое выражение ЗДМ будет записываться:
K × C A m × C B n
K × [A] m × [B] n ,
где k – константа скорости химической реакции, представляющая собой скорость химической реакции при концентрации реагирующих веществ 1моль/л. В отличие от скорости химической реакции, k не зависит от концентрации реагирующих веществ. Чем выше k, тем быстрее протекает реакция.
Зависимость скорости химической реакции от температуры определяется правилом Вант-Гоффа. Правило Вант-Гоффа: при повышении температуры на каждые десять градусов скорость большинства химических реакций увеличивается примерно в 2 – 4 раза. Математическое выражение:
(T 2) = (T 1) × (T2-T1)/10 ,
где – температурный коэффициент Вант-Гоффа, показывающий во сколько раз увеличилась скорость реакции при повышении температуры на 10 o С.
Молекулярность и порядок реакции
Молекулярность реакции определяется минимальным числом молекул, одновременно вступающих во взаимодействие (участвующих в элементарном акте). Различают:
— мономолекулярные реакции (примером могут служить реакции разложения)
N 2 O 5 = 2NO 2 + 1/2O 2
K × C, -dC/dt = kC
Однако, не все реакции, подчиняющиеся этому уравнению мономолекулярны.
— бимолекулярные
CH 3 COOH + C 2 H 5 OH = CH 3 COOC 2 H 5 + H 2 O
K × C 1 × C 2 , -dC/dt = k × C 1 × C 2
— тримолекулярные (встречаются очень редко).
Молекулярность реакции определяется ее истинным механизмом. По записи уравнения реакции определить ее молекулярность нельзя.
Порядок реакции определяется по виду кинетического уравнения реакции. Он равен сумме показателей степеней концентрации в этом уравнении. Например:
CaCO 3 = CaO + CO 2
K × C 1 2 × C 2 – третий порядок
Порядок реакции может быть дробным. В таком случае он определяется экспериментально. Если реакция протекает в одну стадию, то порядок реакции и ее молекулярность совпадают, если в несколько стадий, то порядок определяется самой медленной стадией и равен молекулярности этой реакции.
Примеры решения задач
ПРИМЕР 1